Bu məqalənin sonunda mənbə siyahısı var, lakin mətndaxili mənbələr heç və ya kifayət qədər istifadə edilmədiyi üçün bəzi məlumatların mənbəsi bilinmir. |
Aseton (dimetilketon, propanon-2, YUPAK: propan-2-on) [4] – üzvi maddədir, formulu CH3—C(O)—CH3, doymuş ketonların ən sadə nümayəndəsidir. Aseton adını latınca, asetum — sirkə, adından almışdır. Bu onunla əlaqədardır ki, əvvəllər asetonu asetatlardan alırdılar, asetondan isə sintetik buzlu sirtkə turşusunu alırdılar. 1848-ci ildə Alman tibb və kimya professoru , Latın asetumundan da kök götürən köhnə Alman "Aketon" sözündən (keton, aseton) istifadə edərək, termini rəsmi istifadəyə verdi [5] [6].
| Aseton | |
|---|---|
 | |
 | |
| Ümumi | |
| Ənənəvi adı | aseton, dimetilketon |
| Kimyəvi formulu | C3H6O |
| Molyar kütlə | 58,08 q/mol |
| Fiziki xassələri | |
| Sıxlıq | 0,7899 q/sm³ |
| Termik xüsusiyyətlər | |
| Ərimə nöqtəsi | −95 °S |
| Qaynama nöqtəsi | 56,1 °S |
| 465 °C | |
| Buxarın təzyiqi | 23.998 Pa |
| Kimyəvi xassələri | |
| 19,16 ± 0,04 | |
| Optik xüsusiyyətlər | |
| 1,3588 | |
| Təsnifatı | |
| CAS-da qeyd. nöm. | 67-64-1 |
| PubChem | 180 |
| RTECS | AL3150000 |
| ChEBI | 15347 |
| BMT nömrəsi | 1090 |
| ChemSpider | 175 |
Kəşfi

Andreas Libavius – ilk dəfə asetonu kəşf etmişdir. Ketonların ən sadə və eyni zamanda ən vacib nümayəndəsi olan aseton ilk dəfə 1595-ci ildə alman kimyaçısı Andreas Libavius tərəfindən qurğuşun asetatın quru distillə edilməsi zamanı aşkar edilmişdir. Ancaq yalnız 1832-ci ildə Jean-Baptiste Dumas və Justus von Liebig onun təbiətini və kimyəvi tərkibini dəqiq təyin edə bildilər. 1914-cü ilə qədər aseton, demək olar ki, yalnız ağacın kokslaşmasından əldə edilirdi, lakin Birinci Dünya Müharibəsi illərində ona artan tələbat çox tez bir zaamanda yeni istehsal üsullarının yaradılmasına təkan verdi.
Fiziki xassələri
Aseton xarakterik kəskin qoxusu olan rəngsiz, yanıcı, axıcı, uçucu bir mayedir (n.ş.). Bütün nisbətlərdə su, dietil efiri, benzol, metanol, etanol, bir çox mürəkkəb efirlər və s. ilə qarışır. Ən geniş istifadə edilən həlledici olub, yağları, qatranları və digər maddələri yaxşı həll edir. Asetonun əsas termodinamiki xassələri: [7].
- Səthi gərilmə (20 °C): 23,7 mN/m
- Standart entalpiyası ΔH (298 К): −247,7 кC/Mol
- Standart entrapiyası S (298 К): 200 C/mol•K
- Standart istilik tutumu Orta (298 К): 125 C/mol•K
- Ərimə entalpiyası ΔHər: 5,69 кC/mol
- Qaynama entalpiyası ΔHqay: 29,1 кC/mol
- Yanma istiliyi Qp: 1829,4 кC/mol
- Kritik təzyiq: 4,7 МPa
- Kritik sıxlıq 0,273 q/sm3
- Dinamiki özlülüyü:
o0,36 mPa•s (10 °C) o0,295 mPa•s (25 °C) o0,28 mPa•s (41 °C) Termomexaniki xassələri:
- Havada alışma temperaturu[8]: (-20 °C)[4]
- Havada öz-özünə alışma temperaturue[8][7]: 465 °C
- Partlayıcı qatılığının həddləri[8]: 2,6–12,8 %
Optiki xassələri:
- Şüasındırma əmsalı:
o 1,3591 (20 °C) o 1,3588 (25 °C)
- Dissosasiya əmsalı: pKa = 20 (20 °C, su)
- Dielektrik keçiriciliyi (20 °C): 20,9
- Molekulun dipol mamenti (20 °C): 2,84 Debay Aseton bir cox üzvi maddələri, xüsusilə, asetil- və nitrosellilozaları, alkaloidləri və s., həmçinin bir sıra duzları yaxçı həll edir.
Kimyəvi xassələri
Aseton ən reaksiyaya qabil ketonlardan biridir. Belə ki, o, bisulfit birləşməsi əmələ gətirən bir neçə ketondan biridir:
: ![image]()
Qələvilərin təsiri altında, diaseton spirtinin alınması ilə nəticələnən aldol kondensləşmə reaksiyasına daxil olur:
: ![image]()
Sinkin iştirakı ilə pinakona reduksiya olunur:
: ![image]()
Pirolizindən (7000C) keten alınır:
: ![image]()
Asanlıqla hidrogecianidi özünə birləşdirərək asetonsianhidrin əmələ gətirir:
: ![image]()
Asetonda olan hidrogen atomları asanlıqla halogenlərlə əvəz olunur. Xlorun (yodun) təsiri altında qələvi iştirakı ilə xloroform (yodoform) alınır:
![image]()
Dimetilketonun təyini reaksiyası, onun qələvi mühitində natrium nitroprussid ilə intensiv qirmızı rəngin verməsidir. CH3COOH əlavə etdikdə rəng qırmızı bənövşəyi rəngə dəyişir. 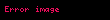
Aseton gümüş güzgü reaksiyasını vermir və polimerləşmir. Bu xassəyə görə ketonlar aldehidlərdən fərqlənir.
Alınması
Dünyada asetonun istehsalı hər il 6.9 milyon ton artır (2012-ci ilə görə [9].) və durmadan artmaqdadır [9]. Sənayedə, birbaşa və ya dolayı yolla propandan alınır.
Kumol üsulu
Asetonun əsas hissəsi benzoldan fenolun kumol üsulu ilə alınmasında ortaq məhsul şəklində əldə edilir. Proses 3 mərhələdə gedir [10]. Birinci mərhələdə benzol propen ilə alkilləşərək kumol alınır, ikinci və üçüncü mərhələdə alınan kumol (Udris – Serqeyev reaksiyası) havanın oksigeni ilə hidroperoksidə qədər oksidləşir, hansı ki, sulfat turşusunun təsirindən fenol və asetona parçalanır:
İzopropanoldan
Bu üsula görə izopropanol buxar fazada katalizator (metal mis, gümüş, nikel, platin) iştirakı ilə 450–6500C temperaturda oksidləşir.
Propenin oksidləşməsindən
Aseton, 50–1200C temperatur və 50–100 atm təzyiqində Pd, Cu, Fe duzlarının mühitində PdCl2 iştirakı ilə mye fazada propenin birbaşa oksidləşməsi ilə əldə edilir:
Clostridium acetobutylicum bakteriyalarının təsiri altında nişastanın mayalandırılması metodu ilə aseton butanolun alınması bəzi əhəmiyyət kəsb edir [11]. Metod az çıxımla xarakterizə olunur. Həmçinin izopripil spirti və asetondan alınması metodundan da istifadə olunur.
Tətbiqi
Aseton bir çox əhəmiyyətli – sirkə anhidridi, ketondiaseton spirti, mesitil oksidi, metil izobutil keton, metil metakrilat, difenilpropan, izoforon, bisfenol və s. məhsulların sintezi üçün xammal kimi istifadə olunur, məs.
Axırıncı polikarbonat, poliuretan və epoksid qətranlarının sintezində geniş istifadə olunur. Aseton, eyni zamanda, yaxşı həlledicidir. əsasən həlledici kimi istifada olunur:
- Lakların istehsalında;
- Partlayıcı maddələrin istehsalında;
- Dərman preparatlarının istehsalında;
- Müxtəlif istehsal proseslərində səthlərin təmizlənməsi üçün komponent və s. Aseton olmadan, asetileni kompakt (mayeləşdirilmiş və silindirli) vəziyyətdə saxlamaq mümkünn deyil, çünki təzyiq altında təmiz formada olduqca partlayıcıdır. Bunun üçün aseton ilə hopdurulmuş məsaməli material olan qablardan istifadı olunur. 1 litr aseton 250 litrə qədər asetileni həll edir. Aseton, həmçinin, bir cox bitki tərkibli maddələrin ekstraksiyasında istifadə olunur. Yanğın təhlükəsi Asetonla işləyərkən əsas təhlükələrdən biri onun asanlıqla alovlanmasıdır. Avtomatik alovlanma temperaturu +4650C, yanma nöqtəsi −200C-dir. Tərkibində 2,5%-dən 12,8%-ə qədər olan hava qarışıqları partlayıcıdır. Bunu nəzərə almalıyıq, çünkü aseton tez buxarlanır və əmələ gələn buxar yanma yerinə qədər (istilik və ya qığılcım) yayıla bilər.
Qeydlər
- http://www.cdc.gov/niosh/ipcsneng/neng0087.html
- ↑ Перейти обратно:1 2 3 http://www.cdc.gov/niosh/npg/npgd0004.html
- ↑ Chiang Y., A. Jerry Kresge, Tang Y. S. et al. The pKa and keto-enol equilibrium constant of acetone in aqueous solution // J. Am. Chem. Soc. / P. J. Stang — American Chemical Society, 1984. — Vol. 106, Iss. 2. — P. 460–462. — ISSN 0002–7863; 1520–5126; 1943–2984 — doi:10.1021/JA00314A055
- ↑ Перейти обратно:1 2 Химическая энциклопедия. — М: Советская энциклопедия, 1988. — Т. 1. — С. 230. — 625 с.
- ↑ Контроль бета-кетонов.
- ↑ Ацетон (кетоновые тела) в моче.
- ↑ Перейти обратно:1 2 Рабинович В. А., Хавин З. Я. Краткий химический справочник: Справ. изд. / Под ред. Потехина А. А., Ефимова А. И.. — Издание 3-е, переработанное и дополненное. — Л.:: Химия, 1991. — С. 328–329. — 432 с. — ISBN 5–7245-0703-X.
- ↑ Перейти обратно:1 2 3 Lewis R. J. Sax's Dangerous Properties of Industrial Materials. — 11ed.. — Wiley-interscience, 2004. — С. 22–23.
- ↑ Перейти обратно:1 2 http://www.newchemistry.ru/printletter.php?n_id=4886ПРОИЗВОДСТВО АЦЕТОНА: получение, применение, рынок по данным АКПР (Академии конъюнктуры промышленных рынков)
- ↑ Химическая энциклопедия. М. 1988, Т1, стр. 230
- ↑http://kodomo.cmm.msu.ru/~ramil.mintaev/projects/C.acetobutylicum/index.php Ацито-бутановая бактерия
Mənbə
- Ацетон // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890–1907.
- Ацетонемия // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890–1907.
- Ацетоновая кислота // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890–1907.
- ГОСТ 2768–84. Ацетон технический. Технические условия.
- http://www.cdc.gov/niosh/ipcsneng/neng0087.html.
- Chiang Y., Kresge A. J., Tang Y. S., Wirz J. The pKa and keto-enol equilibrium constant of acetone in aqueous solution (ing.). // J. Am. Chem. Soc. / P. J. Stang ACS, 1984. Vol. 106, Iss. 2. P. 460–462. ISSN 0002-7863; 1520-5126; 1943-2984 doi:10.1021/JA00314A055
wikipedia, oxu, kitab, kitabxana, axtar, tap, meqaleler, kitablar, oyrenmek, wiki, bilgi, tarix, tarixi, endir, indir, yukle, izlə, izle, mobil, telefon ucun, azeri, azəri, azerbaycanca, azərbaycanca, sayt, yüklə, pulsuz, pulsuz yüklə, haqqında, haqqinda, məlumat, melumat, mp3, video, mp4, 3gp, jpg, jpeg, gif, png, şəkil, muisiqi, mahnı, kino, film, kitab, oyun, oyunlar, android, ios, apple, samsung, iphone, pc, xiomi, xiaomi, redmi, honor, oppo, nokia, sonya, mi, web, computer, komputer
Bu meqalenin sonunda menbe siyahisi var lakin metndaxili menbeler hec ve ya kifayet qeder istifade edilmediyi ucun bezi melumatlarin menbesi bilinmir Lutfen menbeleri uygun sekilde metnin daxilinde yerlesdirerek meqalenin tekmillesdirilmesine komek edin Aseton dimetilketon propanon 2 YUPAK propan 2 on 4 uzvi maddedir formulu CH3 C O CH3 doymus ketonlarin en sade numayendesidir Aseton adini latinca asetum sirke adindan almisdir Bu onunla elaqedardir ki evveller asetonu asetatlardan alirdilar asetondan ise sintetik buzlu sirtke tursusunu alirdilar 1848 ci ilde Alman tibb ve kimya professoru Latin asetumundan da kok goturen kohne Alman Aketon sozunden keton aseton istifade ederek termini resmi istifadeye verdi 5 6 AsetonUmumiEnenevi adi aseton dimetilketonKimyevi formulu C3H6OMolyar kutle 58 08 q molFiziki xasseleriSixliq 0 7899 q sm Termik xususiyyetlerErime noqtesi 95 SQaynama noqtesi 56 1 S465 CBuxarin tezyiqi 23 998 PaKimyevi xasseleripKa displaystyle pK a 19 16 0 04Optik xususiyyetler1 3588TesnifatiCAS da qeyd nom 67 64 1PubChem 180RTECS AL3150000ChEBI 15347BMT nomresi 1090ChemSpider 175KesfiAndreas Libavius ilk defe asetonu kesf etmisdir Andreas Libavius ilk defe asetonu kesf etmisdir Ketonlarin en sade ve eyni zamanda en vacib numayendesi olan aseton ilk defe 1595 ci ilde alman kimyacisi Andreas Libavius terefinden qurgusun asetatin quru distille edilmesi zamani askar edilmisdir Ancaq yalniz 1832 ci ilde Jean Baptiste Dumas ve Justus von Liebig onun tebietini ve kimyevi terkibini deqiq teyin ede bildiler 1914 cu ile qeder aseton demek olar ki yalniz agacin kokslasmasindan elde edilirdi lakin Birinci Dunya Muharibesi illerinde ona artan telebat cox tez bir zaamanda yeni istehsal usullarinin yaradilmasina tekan verdi Fiziki xasseleriAseton xarakterik keskin qoxusu olan rengsiz yanici axici ucucu bir mayedir n s Butun nisbetlerde su dietil efiri benzol metanol etanol bir cox murekkeb efirler ve s ile qarisir En genis istifade edilen helledici olub yaglari qatranlari ve diger maddeleri yaxsi hell edir Asetonun esas termodinamiki xasseleri 7 Sethi gerilme 20 C 23 7 mN m Standart entalpiyasi DH 298 K 247 7 kC Mol Standart entrapiyasi S 298 K 200 C mol K Standart istilik tutumu Orta 298 K 125 C mol K Erime entalpiyasi DHer 5 69 kC mol Qaynama entalpiyasi DHqay 29 1 kC mol Yanma istiliyi Qp 1829 4 kC mol Kritik tezyiq 4 7 MPa Kritik sixliq 0 273 q sm3 Dinamiki ozluluyu o0 36 mPa s 10 C o0 295 mPa s 25 C o0 28 mPa s 41 C Termomexaniki xasseleri Havada alisma temperaturu 8 20 C 4 Havada oz ozune alisma temperaturue 8 7 465 C Partlayici qatiliginin heddleri 8 2 6 12 8 Optiki xasseleri Suasindirma emsali o 1 3591 20 C o 1 3588 25 C Dissosasiya emsali pKa 20 20 C su Dielektrik keciriciliyi 20 C 20 9 Molekulun dipol mamenti 20 C 2 84 Debay Aseton bir cox uzvi maddeleri xususile asetil ve nitrosellilozalari alkaloidleri ve s hemcinin bir sira duzlari yaxci hell edir Kimyevi xasseleriAseton en reaksiyaya qabil ketonlardan biridir Bele ki o bisulfit birlesmesi emele getiren bir nece ketondan biridir CH3 2CO NaHSO3 CH3 2C OH SO3Na displaystyle mathsf CH 3 2 CO NaHSO 3 longrightarrow CH 3 2 C OH SO 3 Na Qelevilerin tesiri altinda diaseton spirtinin alinmasi ile neticelenen aldol kondenslesme reaksiyasina daxil olur 2 CH3 2CO OH CH3 2C OH CH2C O CH3 displaystyle mathsf 2 CH 3 2 CO xrightarrow OH CH 3 2 C OH CH 2 C O CH 3 Sinkin istiraki ile pinakona reduksiya olunur 2 CH3 2CO Zn CH3 2C OH C OH CH3 2 displaystyle mathsf 2 CH 3 2 CO xrightarrow Zn CH 3 2 C OH C OH CH 3 2 Pirolizinden 7000C keten alinir CH3 2CO CH2 C O CH4 displaystyle mathsf CH 3 2 CO longrightarrow CH 2 text C text O CH 4 Asanliqla hidrogecianidi ozune birlesdirerek asetonsianhidrin emele getirir CH3 2CO HCN CH3 2C OH CN displaystyle mathsf CH 3 2 CO HCN longrightarrow CH 3 2 C OH CN Asetonda olan hidrogen atomlari asanliqla halogenlerle evez olunur Xlorun yodun tesiri altinda qelevi istiraki ile xloroform yodoform alinir Hal2 2NaOH NaHal NaOHal H2O displaystyle ce Hal2 2NaOH gt NaHal NaOHal H2O CH3 2CO 3NaOHal CH3 CO CHal3 3NaOH displaystyle ce CH3 2CO 3NaOHal gt CH3 CO CHal3 3NaOH CH3 CO CHal3 NaOH CHHal3 CH3COONa displaystyle ce CH3 CO CHal3 NaOH gt CHHal3 downarrow CH3COONa Dimetilketonun teyini reaksiyasi onun qelevi muhitinde natrium nitroprussid ile intensiv qirmizi rengin vermesidir CH3COOH elave etdikde reng qirmizi benovseyi renge deyisir CH3 2CO Na2 Fe CN 5NO 2NaOH Na4 Fe CN 5ON CHCOCH3 2H2O displaystyle ce CH3 2CO Na2 Fe CN 5NO 2NaOH gt Na4 Fe CN 5ON CHCOCH3 2H2O Aseton gumus guzgu reaksiyasini vermir ve polimerlesmir Bu xasseye gore ketonlar aldehidlerden ferqlenir AlinmasiDunyada asetonun istehsali her il 6 9 milyon ton artir 2012 ci ile gore 9 ve durmadan artmaqdadir 9 Senayede birbasa ve ya dolayi yolla propandan alinir Kumol usulu Asetonun esas hissesi benzoldan fenolun kumol usulu ile alinmasinda ortaq mehsul seklinde elde edilir Proses 3 merhelede gedir 10 Birinci merhelede benzol propen ile alkilleserek kumol alinir ikinci ve ucuncu merhelede alinan kumol Udris Serqeyev reaksiyasi havanin oksigeni ile hidroperokside qeder oksidlesir hansi ki sulfat tursusunun tesirinden fenol ve asetona parcalanir C6H6 CH3CH CH2 C6H5CH CH3 2 displaystyle mathsf C 6 H 6 CH 3 CH text CH 2 longrightarrow C 6 H 5 CH CH 3 2 C6H5CH CH3 2 O2 C6H5C OOH CH3 2 displaystyle mathsf C 6 H 5 CH CH 3 2 O 2 longrightarrow C 6 H 5 C OOH CH 3 2 C6H5C OOH CH3 2 C6H5OH CH3 2CO displaystyle mathsf C 6 H 5 C OOH CH 3 2 longrightarrow C 6 H 5 OH CH 3 2 CO Izopropanoldan Bu usula gore izopropanol buxar fazada katalizator metal mis gumus nikel platin istiraki ile 450 6500C temperaturda oksidlesir CH3 2CH OH O2 CH3 2CO H2O2 displaystyle mathsf CH 3 2 CH text OH O 2 longrightarrow CH 3 2 CO H 2 O 2 Propenin oksidlesmesinden Aseton 50 1200C temperatur ve 50 100 atm tezyiqinde Pd Cu Fe duzlarinin muhitinde PdCl2 istiraki ile mye fazada propenin birbasa oksidlesmesi ile elde edilir CH3CH CH2 PdCl2 H2O CH3 2CO Pd 2HCl displaystyle mathsf CH 3 CH text CH 2 PdCl 2 H 2 O longrightarrow CH 3 2 CO Pd 2HCl 2Pd 4HCl O2 2PdCl2 2H2O displaystyle mathsf 2Pd 4HCl O 2 longrightarrow 2PdCl 2 2H 2 O Clostridium acetobutylicum bakteriyalarinin tesiri altinda nisastanin mayalandirilmasi metodu ile aseton butanolun alinmasi bezi ehemiyyet kesb edir 11 Metod az ciximla xarakterize olunur Hemcinin izopripil spirti ve asetondan alinmasi metodundan da istifade olunur TetbiqiAseton bir cox ehemiyyetli sirke anhidridi ketondiaseton spirti mesitil oksidi metil izobutil keton metil metakrilat difenilpropan izoforon bisfenol ve s mehsullarin sintezi ucun xammal kimi istifade olunur mes Axirinci polikarbonat poliuretan ve epoksid qetranlarinin sintezinde genis istifade olunur Aseton eyni zamanda yaxsi helledicidir esasen helledici kimi istifada olunur Laklarin istehsalinda Partlayici maddelerin istehsalinda Derman preparatlarinin istehsalinda Muxtelif istehsal proseslerinde sethlerin temizlenmesi ucun komponent ve s Aseton olmadan asetileni kompakt mayelesdirilmis ve silindirli veziyyetde saxlamaq mumkunn deyil cunki tezyiq altinda temiz formada olduqca partlayicidir Bunun ucun aseton ile hopdurulmus mesameli material olan qablardan istifadi olunur 1 litr aseton 250 litre qeder asetileni hell edir Aseton hemcinin bir cox bitki terkibli maddelerin ekstraksiyasinda istifade olunur Yangin tehlukesi Asetonla isleyerken esas tehlukelerden biri onun asanliqla alovlanmasidir Avtomatik alovlanma temperaturu 4650C yanma noqtesi 200C dir Terkibinde 2 5 den 12 8 e qeder olan hava qarisiqlari partlayicidir Bunu nezere almaliyiq cunku aseton tez buxarlanir ve emele gelen buxar yanma yerine qeder istilik ve ya qigilcim yayila biler Qeydlerhttp www cdc gov niosh ipcsneng neng0087 html Perejti obratno 1 2 3 http www cdc gov niosh npg npgd0004 html Chiang Y A Jerry Kresge Tang Y S et al The pKa and keto enol equilibrium constant of acetone in aqueous solution J Am Chem Soc P J Stang American Chemical Society 1984 Vol 106 Iss 2 P 460 462 ISSN 0002 7863 1520 5126 1943 2984 doi 10 1021 JA00314A055 Perejti obratno 1 2 Himicheskaya enciklopediya M Sovetskaya enciklopediya 1988 T 1 S 230 625 s Kontrol beta ketonov Aceton ketonovye tela v moche Perejti obratno 1 2 Rabinovich V A Havin Z Ya Kratkij himicheskij spravochnik Sprav izd Pod red Potehina A A Efimova A I Izdanie 3 e pererabotannoe i dopolnennoe L Himiya 1991 S 328 329 432 s ISBN 5 7245 0703 X Perejti obratno 1 2 3 Lewis R J Sax s Dangerous Properties of Industrial Materials 11ed Wiley interscience 2004 S 22 23 Perejti obratno 1 2 http www newchemistry ru printletter php n id 4886PROIZVODSTVO ACETONA poluchenie primenenie rynok po dannym AKPR Akademii konyunktury promyshlennyh rynkov Himicheskaya enciklopediya M 1988 T1 str 230 http kodomo cmm msu ru ramil mintaev projects C acetobutylicum index php Acito butanovaya bakteriyaMenbeAceton Enciklopedicheskij slovar Brokgauza i Efrona v 86 t 82 t i 4 dop SPb 1890 1907 Acetonemiya Enciklopedicheskij slovar Brokgauza i Efrona v 86 t 82 t i 4 dop SPb 1890 1907 Acetonovaya kislota Enciklopedicheskij slovar Brokgauza i Efrona v 86 t 82 t i 4 dop SPb 1890 1907 GOST 2768 84 Aceton tehnicheskij Tehnicheskie usloviya http www cdc gov niosh ipcsneng neng0087 html Chiang Y Kresge A J Tang Y S Wirz J The pKa and keto enol equilibrium constant of acetone in aqueous solution ing J Am Chem Soc P J Stang ACS 1984 Vol 106 Iss 2 P 460 462 ISSN 0002 7863 1520 5126 1943 2984 doi 10 1021 JA00314A055
 Azərbaycanca
Azərbaycanca Deutsch
Deutsch 日本語
日本語 Lietuvos
Lietuvos සිංහල
සිංහල Türkçe
Türkçe Українська
Українська United State
United State