Barium xlorid (BaCl2) ― duzlar sinfinə aid qeyri-üzvi birləşmə. Barium xlorid rəngsiz, romb şəklində olan kristaldır.
| Barium xlorid | |
|---|---|
 | |
 | |
| Ümumi | |
| Kimyəvi formulu | BaCl₂ |
| Molyar kütlə | 0 kq |
| Fiziki xassələri | |
| Sıxlıq | 3,92 (20 °C) q/sm³ |
| Termik xüsusiyyətlər | |
| Ərimə nöqtəsi | 962 °S |
| Qaynama nöqtəsi | 1560 °S |
| Təsnifatı | |
| CAS-da qeyd. nöm. | 10361-37-2 |
| PubChem | 25204, 5360350, 139046011 |
| RTECS | CQ8750000 |
| ChEBI | 63317 |
| BMT nömrəsi | 1564 |
| ChemSpider | 23540 |
Alınması
- Bariumun xlor ilə reaksiyası zamanı:

- Barium oksidin xlorid turşusu ilə reaksiyası zamanı:
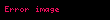
- Barium hidroksidin xlorid turşusu ilə reaksiya zamanı:

- Barium sulfidin kalsium xlorid ilə reaksiya zamanı:

- Barium karbonatin xlorid turşusu ilə reaksiya zamanı:
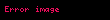
Kimyəvi xassələri
Barium xlorid suda yaxşı, spirtdə az miqdarda, dietil efirində tamami ilə həll olunmur. Barium xlorid duzlarla dəyişmə reaksiyalarına yalnız həll olunmayan bir maddə, qaz halında və ya bir qədər az dissosiasiya olun birləşmə alınanda daxil olur:
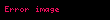
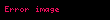
Müəyyən turşular ilə reaksiyaya daxil olur:

Tətbiqi
Barium xlorid kənd təsərrüfatında bitki zərərvericilərinin məhv edilməsi üçün istifadə olunur. Analitik kimyada məhlullarda sulfat turşusu və ya sulfatları aşkar etmək üçün (ağ çöküntü əmələ gəlir) tətbiq olunur. Keramik məhsuları hazırlamaq üçün istifadə olunan kütlənin tərkibinə daxil olur. Kimya sənayesində bariy duzları və bariy əsaslı reaktivlərin istehsalı üçün istifadə olunur.
Toksikliyi
Barium xlorid – toksik maddədir. Dəri və gözlərə düşdükdə, kimyəvi yanığlara səbəb ola bilər, yanğın və partlayışa davamlıdır. Buxarıyla nəfəs aldıqda öskürək, boğazda ağrı baş verir. Daxilə düşdükdə sinir sisteminə, ürəyə pis təsir görsədir. Siçovullar üçün ölümcül dozası daxilə düşdükdə 50-149,2 mq / kq-dır. Barium xloridi qaranlıq otaqda polietilen torbalarda saxlamaq lazımdır. Təmin etmək lazımdır ki, su ilə təmasda olmasın.
İstinadlar
- Рабинович В.А., Хавин З.Я. "Краткий химический справочник" Л.: Химия, 1977 стр. 55
- Ахметов Т.Г. Химия и технология соединений бария. - М.: Химия, 1974. - С. 26-45
- Вредные химические вещества: Неорганические соединения элементов I-IV групп. Справочник. - Л.: Химия, 1988. - С. 136
Mənbə
- [www.xumuk.ru/spravochnik/383.html Хлорид бария на XuMuK.Ru]
- [www.xumuk.ru/encyklopedia/475.html Описание и применение хлорида бария на XuMuK.Ru]
- Barium dichloride (ing.).
wikipedia, oxu, kitab, kitabxana, axtar, tap, meqaleler, kitablar, oyrenmek, wiki, bilgi, tarix, tarixi, endir, indir, yukle, izlə, izle, mobil, telefon ucun, azeri, azəri, azerbaycanca, azərbaycanca, sayt, yüklə, pulsuz, pulsuz yüklə, haqqında, haqqinda, məlumat, melumat, mp3, video, mp4, 3gp, jpg, jpeg, gif, png, şəkil, muisiqi, mahnı, kino, film, kitab, oyun, oyunlar, android, ios, apple, samsung, iphone, pc, xiomi, xiaomi, redmi, honor, oppo, nokia, sonya, mi, web, computer, komputer
Barium xlorid BaCl2 duzlar sinfine aid qeyri uzvi birlesme Barium xlorid rengsiz romb seklinde olan kristaldir Barium xloridUmumiKimyevi formulu BaCl Molyar kutle 0 kqFiziki xasseleriSixliq 3 92 20 C q sm Termik xususiyyetlerErime noqtesi 962 SQaynama noqtesi 1560 STesnifatiCAS da qeyd nom 10361 37 2PubChem 25204 5360350 139046011RTECS CQ8750000ChEBI 63317BMT nomresi 1564ChemSpider 23540AlinmasiBariumun xlor ile reaksiyasi zamani Ba Cl2 BaCl2 displaystyle mathsf Ba Cl 2 longrightarrow BaCl 2 Barium oksidin xlorid tursusu ile reaksiyasi zamani BaO 2HCl BaCl2 H2O displaystyle mathsf BaO 2HCl longrightarrow BaCl 2 H 2 O Barium hidroksidin xlorid tursusu ile reaksiya zamani Ba OH 2 2HCl BaCl2 2H2O displaystyle mathsf Ba OH 2 2HCl longrightarrow BaCl 2 2H 2 O Barium sulfidin kalsium xlorid ile reaksiya zamani BaS CaCl2 BaCl2 CaS displaystyle mathsf BaS CaCl 2 longrightarrow BaCl 2 CaS Barium karbonatin xlorid tursusu ile reaksiya zamani BaCO3 2HCl BaCl2 H2O CO2 displaystyle mathsf BaCO 3 2HCl longrightarrow BaCl 2 H 2 O CO 2 uparrow Kimyevi xasseleriBarium xlorid suda yaxsi spirtde az miqdarda dietil efirinde tamami ile hell olunmur Barium xlorid duzlarla deyisme reaksiyalarina yalniz hell olunmayan bir madde qaz halinda ve ya bir qeder az dissosiasiya olun birlesme alinanda daxil olur BaCl2 MgSO4 BaSO4 MgCl2 displaystyle mathsf BaCl 2 MgSO 4 longrightarrow BaSO 4 downarrow MgCl 2 BaCl2 K2CrO4 BaCrO4 2 KCl displaystyle mathsf BaCl 2 K 2 CrO 4 longrightarrow BaCrO 4 downarrow 2 KCl Mueyyen tursular ile reaksiyaya daxil olur BaCl2 H2SO4 BaSO4 2 HCl displaystyle mathsf BaCl 2 H 2 SO 4 longrightarrow BaSO 4 downarrow 2 HCl TetbiqiBarium xlorid kend teserrufatinda bitki zerervericilerinin mehv edilmesi ucun istifade olunur Analitik kimyada mehlullarda sulfat tursusu ve ya sulfatlari askar etmek ucun ag cokuntu emele gelir tetbiq olunur Keramik mehsulari hazirlamaq ucun istifade olunan kutlenin terkibine daxil olur Kimya senayesinde bariy duzlari ve bariy esasli reaktivlerin istehsali ucun istifade olunur ToksikliyiBarium xlorid toksik maddedir Deri ve gozlere dusdukde kimyevi yaniglara sebeb ola biler yangin ve partlayisa davamlidir Buxariyla nefes aldiqda oskurek bogazda agri bas verir Daxile dusdukde sinir sistemine ureye pis tesir gorsedir Sicovullar ucun olumcul dozasi daxile dusdukde 50 149 2 mq kq dir Barium xloridi qaranliq otaqda polietilen torbalarda saxlamaq lazimdir Temin etmek lazimdir ki su ile temasda olmasin IstinadlarRabinovich V A Havin Z Ya Kratkij himicheskij spravochnik L Himiya 1977 str 55 Ahmetov T G Himiya i tehnologiya soedinenij bariya M Himiya 1974 S 26 45 Vrednye himicheskie veshestva Neorganicheskie soedineniya elementov I IV grupp Spravochnik L Himiya 1988 S 136Menbe www xumuk ru spravochnik 383 html Hlorid bariya na XuMuK Ru www xumuk ru encyklopedia 475 html Opisanie i primenenie hlorida bariya na XuMuK Ru Barium dichloride ing
 Azərbaycanca
Azərbaycanca Беларускі
Беларускі Dansk
Dansk Deutsch
Deutsch Española
Española Français
Français Indonesia
Indonesia Italiana
Italiana 日本語
日本語 Қазақ
Қазақ Lietuvos
Lietuvos Nederlands
Nederlands Português
Português Русский
Русский සිංහල
සිංහල แบบไทย
แบบไทย Türkçe
Türkçe Українська
Українська 中國人
中國人 United State
United State Afrikaans
Afrikaans